Lipid-Nanopartikel
Ihr Vorsprung in der Forschung
Echelon Biosciences ist ein auf Lipide spezialisiertes Unternehmen mit jahrzehntelanger Erfahrung. Auf der Grundlage umfassender Fachkenntnisse in den Bereichen Lipide, Lipidsignalwege und Molekularbiologie ist Echelon nicht nur in der chemischen Synthese von Lipiden versiert, sondern versteht auch, wie diese in einem biologischen Kontext funktionieren.
ist ein auf Lipide spezialisiertes Unternehmen mit jahrzehntelanger Erfahrung. Auf der Grundlage umfassender Fachkenntnisse in den Bereichen Lipide, Lipidsignalwege und Molekularbiologie ist Echelon nicht nur in der chemischen Synthese von Lipiden versiert, sondern versteht auch, wie diese in einem biologischen Kontext funktionieren.
Lipidnanopartikel für den RNA-Transport
Gentherapien werden seit einigen Jahren entwickelt, wobei bereits mehrere DNA-basierte Behandlungen zugelassen sind. Diese stützen sich jedoch häufig auf virale Vektoren, welche Immunreaktionen auslösen können. RNA-basierte Therapien bieten eine vielversprechende Alternative und haben insbesondere nach dem Erfolg von mRNA-Impfstoffen und RNA-Medikamenten in den letzten Jahren an Bedeutung gewonnen.
Eine zentrale Herausforderung besteht darin, dass freie RNA nicht direkt verwendet werden kann, da sie instabil ist, Immunreaktionen auslösen kann und von Zellen nur schlecht aufgenommen wird. Um dies zu beheben, werden Transportsysteme wie Lipidnanopartikel (LNPs) eingesetzt. LNPs schützen die RNA vor dem Abbau und ermöglichen ihr Eindringen in die Zellen, wodurch die kodierten therapeutischen Proteine produziert werden können. Eine wirksame Therapie hängt von der sorgfältigen Gestaltung sowohl der RNA als auch der LNP-Formulierung ab.
Bei der Entwicklung von Lipidnanopartikeln (LNPs) muss ein Gleichgewicht zwischen Wirksamkeit und Immunantwort gefunden werden. Sowohl mRNA als auch die verwendeten ionisierbaren Lipide können eine Immunantwort auslösen – was für Impfstoffe nützlich, für Therapien mit wiederholter Verabreichung, wie beispielsweise die Genbearbeitung, jedoch problematisch ist. PEGylierte Lipide verlängern die Zirkulationszeit, können jedoch Anti-PEG-Antikörper induzieren, was zu einer schnelleren Clearance führt. Alternativen wie Polysarcosin werden untersucht, um dieses Problem zu verringern, ohne die Effizienz zu beeinträchtigen. Eine weitere Herausforderung ist die gezielte Verabreichung: Während Impfstoffe von einer systemischen Verteilung profitieren, erfordern andere Therapien eine zellspezifische Zielerfassung. Zu den Strategien gehören die Modifizierung der Oberflächenladung der LNPs oder die Zugabe von Targeting-Peptiden oder Antikörpern, um sie zu den gewünschten Geweben zu leiten.
RNA-Synthese
Der Großteil der in LNPs verwendeten RNA wird mittels In-vitro-Transkription (IVT) hergestellt, einem flexiblen Verfahren, bei dem je nach RNA-Typ und Sequenzanforderungen unterschiedliche RNA-Polymerasen zum Einsatz kommen. Wichtige Elemente wie UTRs, kodierende Regionen, Ribosomen-Eintrittsstellen und Poly(A)-Schwänze werden entsprechend dem therapeutischen Ziel einbezogen. IVT-mRNA erfordert einen Capping-Schritt, und Faktoren wie Capping-Effizienz, Poly(A)-Addition und Sequenzintegrität werden während der Synthese und Reinigung bewertet. Zudem ist ein Expressionsscreening erforderlich, um zu bestätigen, dass die RNA korrekt translatiert wird und funktionell aktiv ist.
Zu bedenken:
- Der in einem LNP verwendete RNA-Typ ist der erste entscheidende Aspekt bei der Konzeption, da sich siRNA, mRNA und zirkuläre RNA hinsichtlich Länge, Struktur und Sequenzanforderungen unterscheiden. Selbst bei Verwendung der minimal erforderlichen Elemente kann je nach Zielzelle oder -gewebe eine zusätzliche Optimierung erforderlich sein.
- Die RNA-Komponenten werden weitgehend durch den RNA-Typ bestimmt. Bei mRNA sind untranslatierte Regionen (5'- und 3'-UTRs) sowie ein Poly(A)-Schwanz erforderlich, um das Transkript zu stabilisieren und die Translation nach der Verabreichung zu ermöglichen. Während einige Elemente allgemein anwendbar sind, können spezifische UTRs die Expression in bestimmten Zellen verstärken, und eine Codonoptimierung der kodierenden Region kann die Effizienz weiter verbessern.
- mRNA-Moleküle erfordern während der Synthese einen zusätzlichen Capping-Schritt. Eukaryotische Transkripte tragen von Natur aus eine 5'-Cap, ein Nukleotidanalogon, das die Stabilität erhöht und für die Translation unerlässlich ist. Diese Cap kann während der IVT unter Verwendung synthetischer Cap-Analoga hinzugefügt oder in einem späteren Reaktionsschritt nach der Transkription eingeführt werden. Es stehen verschiedene Cap-Analoga zur Verfügung, und bei ihrer Auswahl muss ein Gleichgewicht zwischen Immunogenität und Translationseffizienz gefunden werden.
- Die RNA-Synthese erfolgt typischerweise mittels In-vitro-Transkription (IVT), die eine lineare DNA-Matrize und spezifische Promotorsequenzen erfordert, die die Transkription durch rekombinante RNA-Polymerasen wie T7 ermöglichen. Die IVT ist flexibel, ermöglicht die einfache Einbindung modifizierter Nukleotide und ist skalierbar, sobald die Bedingungen optimiert sind. Matrizen können durch Restriktionsverdau, PCR oder Oligonukleotid-Assemblierung erzeugt werden.
- Die RNA-Analyse erfolgt vor und nach der LNP-Verkapselung. Das Transkript wird zunächst durch Chromatographie gereinigt, um überschüssige Nukleotide zu entfernen und die Reinheit zu beurteilen, gefolgt von einer Überprüfung der korrekten Länge und Sequenz. Nach der Bestätigung wird die RNA zu LNPs formuliert, und ihre Integrität wird erneut überprüft, um sicherzustellen, dass während der Verkapselung kein Abbau oder keine Fragmentierung stattgefunden hat.
LNP-Formulierung
Eine erfolgreiche LNP-Formulierung erfordert die Berücksichtigung mehrerer wichtiger Aspekte. Bei der Entwicklung müssen sowohl die Zielzelle oder das Zielgewebe als auch die Effizienz berücksichtigt werden, mit der ionisierbare Lipide die Fracht einkapseln und freisetzen. Die Frachtsynthese sollte Elemente umfassen, die die Stabilität und Expression der Nukleinsäurekomponenten während der Klonierung gewährleisten, und kann modifizierte Nukleotide beinhalten, um die Immunogenität zu verringern.
LNP-Komponenten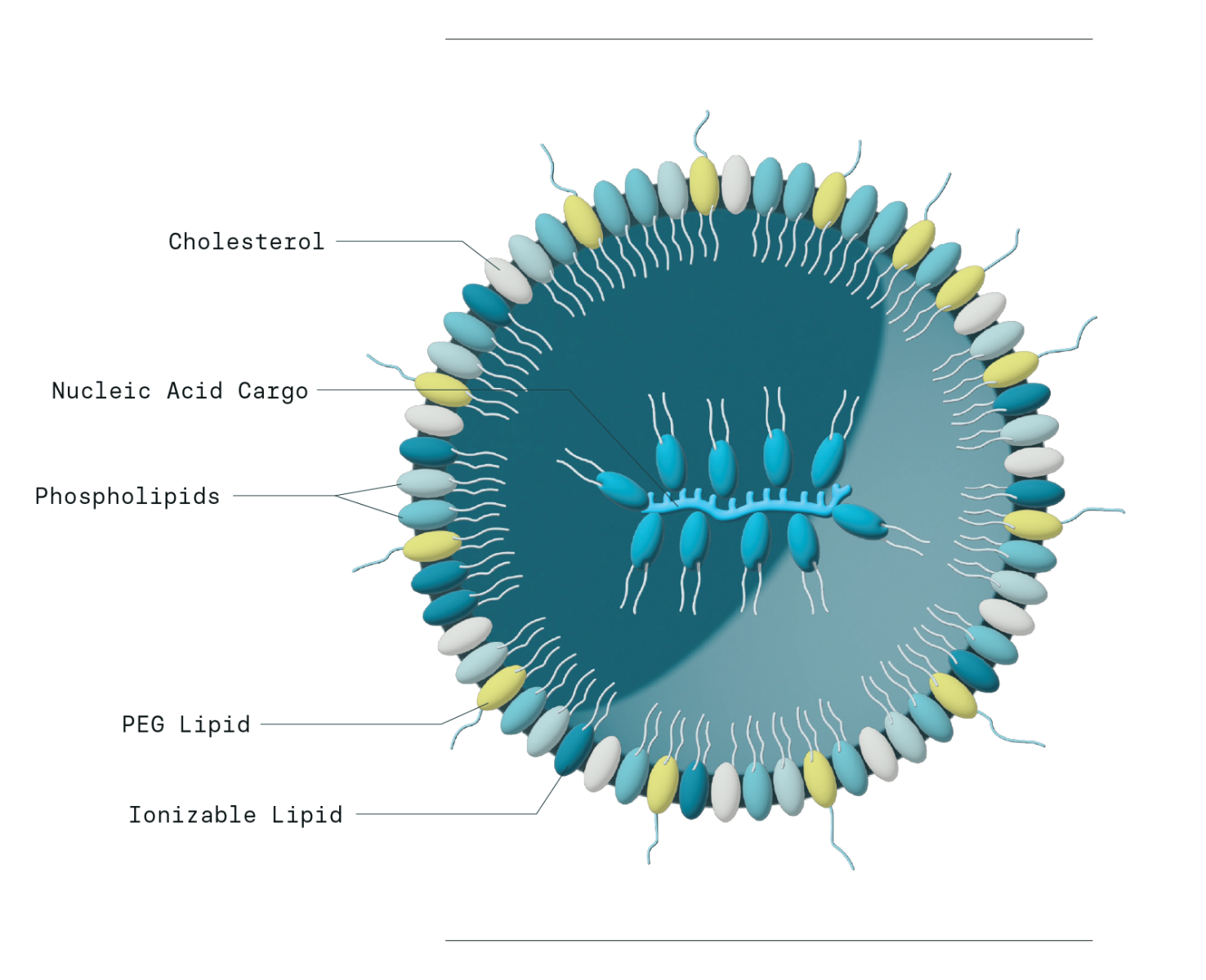
Die Bausteine von LNPs sind bemerkenswert einfach. Ein typisches LNP enthält ein ionisierbares oder kationisches Lipid, Cholesterin, mindestens ein Phospholipid und ein mit Polyethylenglykol (PEG) modifiziertes Lipid. Diese Lipidkomponenten dienen dazu, eine Nukleinsäure-Nutzlast zu schützen oder einzukapseln, die für ein therapeutisches Protein kodiert.
Die Art der Fracht reicht von mRNA oder siRNA bis hin zu Plasmid-DNA.
Die Wahl der Lipide in der Formulierung wird durch die Art der Fracht beeinflusst.
Sobald ausreichend Fracht produziert wurde, wird im Rahmen eines ersten Formulierungs-Screenings bewertet, wie sich verschiedene ionisierbare Lipide und Zusammensetzungen mit der Fracht verbinden. Die nachgelagerte Analyse liefert mehr als nur Daten zur Verkapselung und ist für die Beurteilung des Erfolgs der Formulierung unerlässlich. Schließlich wird ein Expressions-Screening empfohlen, da nicht alle Formulierungen, die die analytischen Prüfungen bestehen, funktionsfähige LNPs hervorbringen.
Zu bedenken:
- Der entscheidende Faktor beim Design der LNPs ist das ionisierbare Lipid, das die Einkapselung und Freisetzung der Ladung steuert und auf die Art der Nukleinsäure (z. B. dsDNA, mRNA, siRNA) abgestimmt sein muss. Die Größe und Oberflächenladung der LNPs lassen sich durch Anpassung der Arten und Verhältnisse von Phospholipiden und PEG-Lipiden weiter optimieren.
- Die Fracht-Synthese für RNA-LNPs erfolgt typischerweise durch In-vitro-Transkription aus einer DNA-Matrize. Bei mRNA werden nicht-kodierende Elemente wie UTRs je nach Zielgewebe oder Zelltyp ausgewählt, um die Stabilität und Translation zu verbessern. Die Auswahl der Cap-Struktur muss ebenfalls im Voraus geplant werden, da sie von spezifischen Sequenzanforderungen am Anfang des Transkripts abhängen kann.
- Sobald die Lipide und die Ladung vorbereitet sind, erfolgt die LNP-Formulierung unter Verwendung automatisierter mikrofluidischer Mischer, um die Reproduzierbarkeit zu gewährleisten. Diese Systeme steuern präzise das schnelle Vermischen der Lipide der organischen Phase mit der wässrigen Ladung und ermöglichen eine flexible Anpassung der Mischungsverhältnisse, was für verschiedene RNA-Typen von Bedeutung sein kann.
- Die initiale LNP-Analyse konzentriert sich auf die Messung der Ladungseinkapselung. Die weitere Charakterisierung umfasst Partikelgröße, Molekulargewicht, Oberflächenladung und Polydispersität. Formulierung und Analyse sind iterative Prozesse während des Screenings, und die Entscheidung, ob eine Formulierung ausreichend ist, hängt von diesen Schlüsselparametern ab.
- Das In-vitro-Expressionsscreening ist ein ergänzender Schritt nach der Formulierung und Analyse. Auch wenn In-vitro- und In-vivo-Ergebnisse nicht immer übereinstimmen, ermöglicht es eine frühzeitige Validierung der LNP-Leistung und kann als Orientierung für das weitere Screening oder die Auswahl für In-vivo-Tests dienen. Die Verwendung von Referenz-LNPs mit bekannter hoher Expression kann die Zuverlässigkeit verbessern.
Ionisierbare Lipide und Hilfslipide für die LNP-Formulierung
Um die Herausforderungen bei der LNP-Entwicklung zu bewältigen, bietet Echelon Biosciences eine Reihe hochwertiger ionisierbarer Lipide und Hilfslipide für Forschungs- und Entwicklungszwecke an.
Ionisierbare Lipide
Ionisierbare Lipide sind die Schlüsselkomponente für den Aufbau eines voll ausgebildeten Lipidnanopartikels. Diese spezialisierten Lipide nehmen bei saurem pH-Wert eine positive Ladung an, wodurch sie mit Nukleinsäuren, die über ihre Phosphatgruppen negative Ladungen tragen, interagieren und diese einkapseln können.
Das Screening und die Auswahl ionisierbarer Lipide richten sich nach der Art der Nukleinsäure-Nutzlast, dem Zielgewebe und der therapeutischen Anwendung.
Der Bedarf an neuen ionisierbaren Lipiden wächst, da die Anzahl der für die Therapie in Frage kommenden Zelltypen und die Vielfalt der RNA-Typen stetig zunehmen. Die Chemiker von Echelon verfügen über langjährige Erfahrung in der Lipidsynthese und erweitern unseren Produktkatalog kontinuierlich um neue ionisierbare Lipide.
Ausgewählte ionisierbare Lipide von Echelon Biosciences
| Produktnr. | Ionisierbares Lipid |
|---|---|
| ECH-N-1003 | AA3-Dlin |
| ECH-N-1007 | LP-01 |
| ECH-N-1010 | 306Oi10 |
| ECH-N-1017 | DOG-IM4 |
| ECH-N-1025 | 6,6’-trehalose dioleate |
| ECH-N-1050 | YSK05 |
| ECH-N-1110 | Lipid 10 |
| ECH-N-1128 | 306-O12B |
| ECH-N-1220 | C12-200 |
| ECH-N-1316 | 306-N16B |
| ECH-N-1319 | Lipid 319 |
| ECH-N-1438 | 4A3-SC8 |
Hilfslipide
Als Hilfslipide werden die übrigen Lipidkomponenten von LNPs bezeichnet, die nicht zum ionisierbaren Lipid gehören. Dazu gehört in der Regel eine Kombination aus Cholesterin, einem Phospholipid und einem PEGylierten Lipid, die die äußere Membranstruktur bildet, welche die von den ionisierbaren Lipiden eingefangenen Nukleinsäuren vollständig umschließt. Die Stabilität und andere physikalisch-chemische Eigenschaften von LNPs lassen sich durch Anpassung der Art und des Verhältnisses dieser Lipide in den verschiedenen LNP-Formulierungen optimieren.
Ausgewählte Helferlipide von Echelon Biosciences
| Produktnr. | Hilfslipid |
|---|---|
| ECH-L-0112 | 9(10)-Nitrooleic Acid |
| ECH-L-1122 | PLPC (16:0/18:2 PC) |
| ECH-L-1182 | DOPC (18:1/18:1 PC) |
| ECH-L-1618 | POPC (16:0/18:1 PC) |
| ECH-L-2116 | DPPE (16:0/16:0 PE) |
| ECH-L-2118 | DSPE (18:0/18:0 PE) |
| ECH-L-2182 | DOPE (18:1/18:1 PE) |
| ECH-L-2810 | DSPE-PEG2000-Maleimide |
| ECH-L-2811 | DSPE-PEG2000-NH2 |
| ECH-L-2814 | DSPE-PEG2000-COOH |
| ECH-L-6004 | 7-Dehydrocholesterol (7-DHC) |
| ECH-L-6005 | Ergosterol |
| ECH-L-6012 | Cholesterol |
Trailblazer LNP-Kits
Die Trailblazer LNP-Kits von Echelon wurden entwickelt, um die Erforschung von LNPs in der Anfangsphase zu vereinfachen. Jedes Kit enthält einen Puffer zur Verdünnung von Nukleinsäuren sowie die zur Bildung von LNPs erforderlichen Lipide, entweder in gefriergetrockneter oder vorgemischter Form.
Das vorgemischte LNP-Kit verwendet für jedes Lipid einen standardisierten molaren Anteil, sodass genaue Vergleiche möglich sind. Das lyophilisierte LNP-Kit ermöglicht es dem Experimentator, das Verhältnis der Lipidkomponenten nach Bedarf anzupassen.
| Produktnr. | LNP-Kit |
|---|---|
| K-6300L | TRAILBLAZER |
| K-6300M | TRAILBLAZER PRE-MIXED |
Wenn Sie eine neuartige ionisierbare oder kationische Lipidstruktur untersuchen möchten, oder wenn ein Artikel nicht in unserem Katalog aufgeführt ist, kontaktieren Sie uns gerne für eine Beratung oder um eine maßgeschneiderte Synthese in Auftrag zu geben.
05.05.2026

SpinMate-Ultrafiltra...
Höhere Effizienz bei der Proteinreinigung

Tumor-Marker
Rekombinante Antikörper von Absolute Antibody
Antikörper-Wirkstoff...
ADC-Konjugationskit von ACROBiosystems
Zelladhäsionsmolekül...
Schlüssel-Targets abgedeckt durch Biorbyt
Single-Domain Antikö...
Überlegene Färbeleistung mit Biotium MiniMab™

