Immun-Checkpoint Marker
Antikörper für die Immunhistochemie
Immun-Checkpoints haben sich als wichtige Ziele für die Krebstherapie etabliert. Bislang haben sich PD-1 und CTLA-4 als die erfolgsversprechensten Immun-Checkpoints für die Entwicklung von Therapeutika erwiesen. Der kürzlich entdeckte TIGIT-Signalweg bietet ein großes therapeutisches Potenzial, insbesondere in Kombination mit anderen Immun-Checkpoint-Inhibitoren.
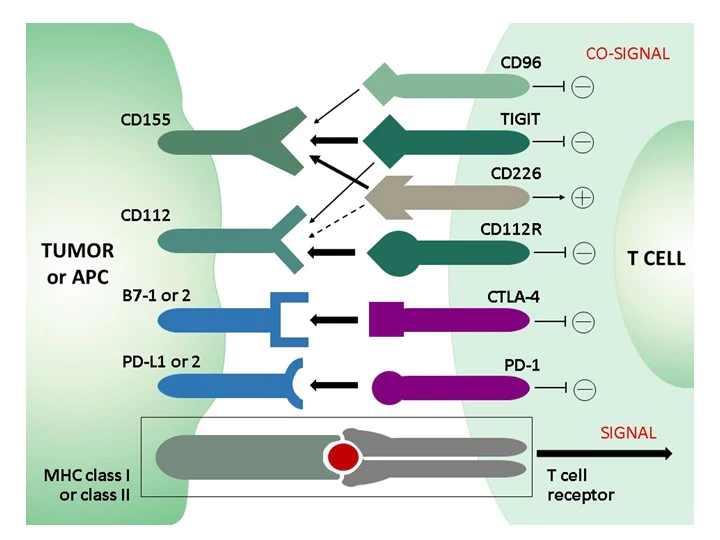 Im gesunden Immunsystem regulieren ko-inhibitorische und ko-stimulatorische Rezeptoren auf den T-Zellen die Stimulation der T-Zell-Rezeptoren (t cell receptors, TCR), um unerwünschte Autoimmunreaktionen zu begrenzen. Während bei einer akuten Infektion CD8-Effektor-T-Zellen nach Beseitigung des Erregers zu Gedächtniszellen werden, führt eine anhaltende Stimulation und Entzündung - entweder durch Nicht-Selbst-Antigene bei einer chronischen Infektion oder durch Selbst-Antigene in der Tumormikroumgebung (TEM) bei Krebs - zu einem fortschreitenden Funktionsverlust der CD8-T-Zellen, der als "T-Zell-Erschöpfung" bezeichnet wird. Ein phänotypisches Merkmal erschöpfter CD8-T-Zellen ist die erhöhte und anhaltende Expression unterschiedlicher Kombinationen von Hemmrezeptoren (Immun-Checkpoints), darunter PD-1, STLA-4, TIM-3, LAG-3 und andere, wie TIGIT oder der kürzlich entdeckte neue Immun-Checkpoint CD112R. Aufgrund der Beteiligung dieser inhibitorischen Rezeptoren an der T-Zell-Dysfunktion wurden neue therapeutische Strategien entwickelt, die darauf abzielen, die hemmenden Rezeptoren mit monoklonalen Antikörpern zu blockieren (Checkpoint-Blockade) und so die T-Zell-Funktion wiederherzustellen.
Im gesunden Immunsystem regulieren ko-inhibitorische und ko-stimulatorische Rezeptoren auf den T-Zellen die Stimulation der T-Zell-Rezeptoren (t cell receptors, TCR), um unerwünschte Autoimmunreaktionen zu begrenzen. Während bei einer akuten Infektion CD8-Effektor-T-Zellen nach Beseitigung des Erregers zu Gedächtniszellen werden, führt eine anhaltende Stimulation und Entzündung - entweder durch Nicht-Selbst-Antigene bei einer chronischen Infektion oder durch Selbst-Antigene in der Tumormikroumgebung (TEM) bei Krebs - zu einem fortschreitenden Funktionsverlust der CD8-T-Zellen, der als "T-Zell-Erschöpfung" bezeichnet wird. Ein phänotypisches Merkmal erschöpfter CD8-T-Zellen ist die erhöhte und anhaltende Expression unterschiedlicher Kombinationen von Hemmrezeptoren (Immun-Checkpoints), darunter PD-1, STLA-4, TIM-3, LAG-3 und andere, wie TIGIT oder der kürzlich entdeckte neue Immun-Checkpoint CD112R. Aufgrund der Beteiligung dieser inhibitorischen Rezeptoren an der T-Zell-Dysfunktion wurden neue therapeutische Strategien entwickelt, die darauf abzielen, die hemmenden Rezeptoren mit monoklonalen Antikörpern zu blockieren (Checkpoint-Blockade) und so die T-Zell-Funktion wiederherzustellen.
Der anhaltende klinische Erfolg von Therapien mit Checkpoint-Inhibitoren gegen PD-1, PD-L1 oder CTLA-4 in Bezug auf das Gesamtüberleben von Krebspatienten beweist das therapeutische Potenzial von Immun-Checkpoints und gibt Anlass zu neuen vielversprechenden Zielen und kombinatorischen Ansätzen für die Immun-Checkpoint-Blockade-Strategien. Ein neueres therapeutisches Ziel ist TIGIT: Monoklonale Antikörper gegen TIGIT blockierten nicht nur dessen hemmende Wirkung, sondern verlagerten auch das Gleichgewicht zugunsten des koaktivierenden Rezeptors CD226, der die TIGIT-Liganden teilt. TIGIT und CD226 bilden einen Signalweg, der dem des koinhibitorischen Rezeptors CTLA-4 und des ko-aktivierenden Rezeptors CD28 ähnelt.
 Für viele dieser Immun-Checkpoint-Zielmoleküle bieten wir unter unserer Marke dianova hochwertige monoklonale Antikörper für die immunhistochemische Anwendung in menschlichem FFPE-Standardtumorgewebe zu diagnostischen Zwecken an.
Für viele dieser Immun-Checkpoint-Zielmoleküle bieten wir unter unserer Marke dianova hochwertige monoklonale Antikörper für die immunhistochemische Anwendung in menschlichem FFPE-Standardtumorgewebe zu diagnostischen Zwecken an.
Neuer Immun-Checkpoint Marker TIGIT
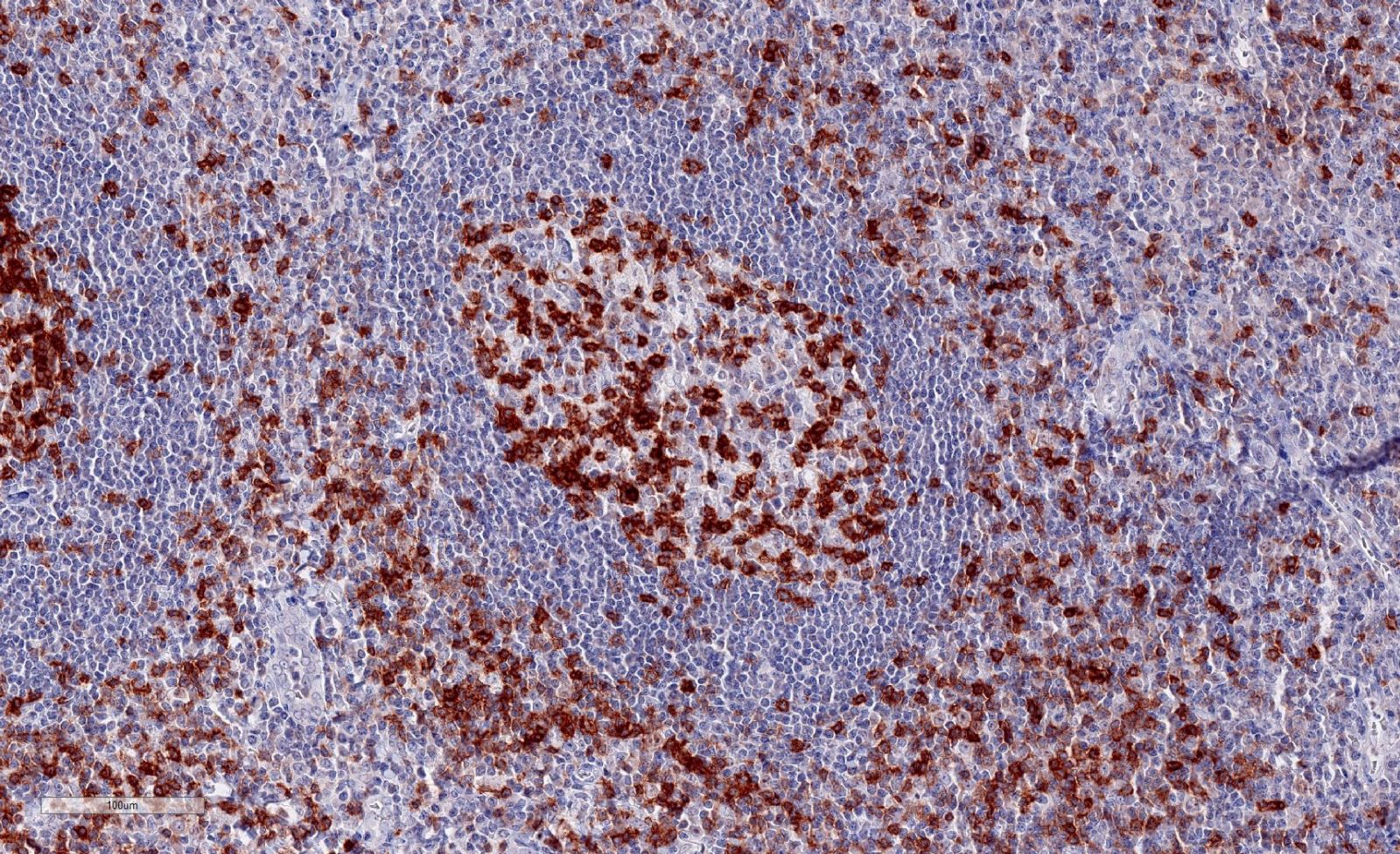
Klon TG1 ist der erste monoklonale Antikörper, der TIGIT (T-Zell-Immunrezeptor mit Ig- und ITIM-Domänen) in standardmäßigen humanen FFPE-Gewebeproben nachweist. Er wurde für die Identifizierung TIGIT-positiver T-Zellen validiert, die menschliche Tumore infiltrieren, um den Nachweis von TIGIT in der Mikroumgebung des Tumors unter pathologischen Bedingungen zu ermöglichen. Die immunhistochemische Anwendung des monoklonalen Antikörpers TG1 kann wertvolle Informationen für die klinische Forschung und potenzielle therapeutische Interventionen liefern, die speziell auf den TIGIT-bezogenen Tumorimmunologie-Checkpoint abzielen.
Annibali et al. veröffentlichten eine Studie über die Entwicklung eines neuen TIGIT-Scoring-Systems für Hodgkin-Lymphome, das auf der Expression von TIGIT, PD-1 und PD-L1 basiert. Zur Analyse der TIGIT-Expression haben sie unseren dianova Anti-TIGIT TG1-Antikörper verwendet.
Niebel et al. untersuchten mit Hilfe unseres dianova Anti-TIGIT TG1-Antikörpers in einer aktuellen Studie die durch DNA-Methylierung regulierte TIGIT-Expression in der Melanom-Mikroumgebung als vielversprechenden Marker für das Überleben von Patienten.
Neuer Immun-Checkpoint Marker CD112R
TIGIT und CD226 bilden einen T-Zell-Ko-Signalweg, in dem CD226 und TIGIT als kostimulatorische bzw. ko-inhibitorische Rezeptoren für die Liganden CD155 und CD112 dienen. Diese TIGIT-Signalachse umfasst ein komplexes Rezeptor-Liganden-System mit dem Marker CD112R, der ein vielversprechendes Ziel für die Krebsimmuntherapie geworden ist. CD112R, ein Mitglied der rezeptorähnlichen Proteine des Poliovirus, wird bevorzugt auf T-Zellen exprimiert und hemmt T-Zell-Rezeptor-vermittelte Signale. Die Blockade der CD112R-CD112-Interaktion verstärkt die T-Zell-Antwort. CD112, der Ligand für CD112R, ist auf Tumorzellen und Antigen-präsentierenden Zellen weit verbreitet. CD112R wirkt als ko-inhibitorischer Rezeptor für T-Zellen, da es mit CD226 um die Bindung an CD112 konkurriert. Die Blockierung der CD112R-CD112-Interaktion verstärkt die Reaktion humaner T-Zellen.
Der Anti-PVRIG/CD112R-Klon R12 wurde für den Nachweis von CD112R in formalinfixierten, in Paraffin eingebetteten Routinegewebeproben (IHC FFPE) entwickelt. Der Klon R12 weist keinen Hintergrund in Epithelzellen und nicht lymphatischen Zellen auf und wurde hinsichtlich seiner Empfindlichkeit und Spezifität in verschiedenen normalen und Tumorgeweben validiert.
Ausgewählte Immun-Checkpoint-Marker-Antikörper für die Immunhistochemie:
| Art. Nr. | Produktbeschreibung |
|---|---|
| DNA-IHC-184010 | Monoklonaler Anti-PD-L1 aus Kaninchen [HL1041] |
| ODN-DIA-R12 | Monoklonaler Anti-CD112R/PVRIG (Hu) aus der Maus [R12] |
| ODN-DIA-TG1-M | Monoklonaler Anti-TIGIT (Hu) aus der Maus [TG1] |
| ODN-DIA-TG2-M | Monoklonaler Anti-TIGIT (Hu) aus der Maus [TG2] |
Das könnte Sie ebenfalls interessieren:
>> News: Adaptive Immunität - HLA-G Antikörper-Panel für die Durchflusszytometrie
>> News: Krebsforschung - LSBio PathPlus™ validierte Antikörper
>> Journal Club: The RANK Pathway as an Immune Modulator in Breast Cancer
26.04.2022

SpinMate-Ultrafiltra...
Höhere Effizienz bei der Proteinreinigung

Tumor-Marker
Rekombinante Antikörper von Absolute Antibody
Antikörper-Wirkstoff...
ADC-Konjugationskit von ACROBiosystems

Lipid-Nanopartikel
Ihr Vorsprung in der Forschung
Zelladhäsionsmolekül...
Schlüssel-Targets abgedeckt durch Biorbyt